Su molekülü hangi atomlara bölünmüştür? Formül, kimyasal reaksiyonlar
Su, dünyadaki yaşamın temel şartıdır. Dünya'nın yüzeyi okyanusların, denizlerin, nehirlerin ve göllerin üçte ikisinden oluşur. Dünyanın okyanuslarındaki su hacmi, tüm arazinin on katıdır.
Dünya, okyanuslardaki bir adadır
Gezegenimiz, kıtaların aslında yalnızca büyük adalar olduğu bir okyanus olarak kabul edilebilir; bunun nedeni, yakın yörüngesel yörüngeden Dünya'nın yeşil-mavi olduğu, okyanusun renginin olduğu görülmesidir.

Gezegenimizdeki her canlı,Örneğin, bir denizanası% 95'i içerir ve insan vücudu% 65 su içerir. Bu maddenin eksikliği vücut ağırlığının sadece% 1'i susuzluk hissi yaratır. Vücut neminin% 10'unu kaybederse ölümüne neden olabilir. Neredeyse tüm kimyasal reaksiyonlar, su ortamında ortaya çıkar. Buharlaşma, su toprak sakinlerinin sıcaklığını düzenler. Bir adam terlemediğinde, bir saat sık çalıştıktan sonra vücut ısısı 46'ya yükselirdiyaklaşıkS.
Su dinamiği
Su ortamı sürekli hareket halindedir: açık rezervlerden, bulutların girmeden, yağmur veya kar gibi düşer ve daha sonra akarsu, nehir ve denize akan dereler buharlaşır. Nem zemine sızar, birikir ve suyu tekrar doldurduğu yüzeye gelir. Suyun büyük kısmı, katı halde, atmosferde buhar olarak mevcut - dağlarda kar ve buz kütlelerinin büyük tabakalar biçiminde ve kutup bölgelerinde. Yağmur suyunun yaklaşık yirminci kısmı doğrudan canlı organizmalar tarafından kullanılır. Doğal su kesinlikle temiz değildir, en saf yağmur olarak kabul edilir, ancak havadan sıkışmış bazı yabancı maddeler vardır.
Şekilde su molekülünün hangi atomlardan oluştuğu ve doğaya nasıl bölündüğü gösterilmektedir.

Suyun yapısı
Su molekülünün hangi atomlara bölündüğü hakkında - bugünlerde herhangi bir öğrenci bilir.
Bu maddenin her molekülü,bir oksijen atomu ve iki hidrojen atomu. Bu, üç unsurun sanki birbirine karşı sanki bir yapıdadır. Oksijen atomunun ortasında (kimyasal simge - O) iki tarafta iki hidrojen atomu (H) bulunur - bunlar su moleküllerinin bölündüğü atomlardır.
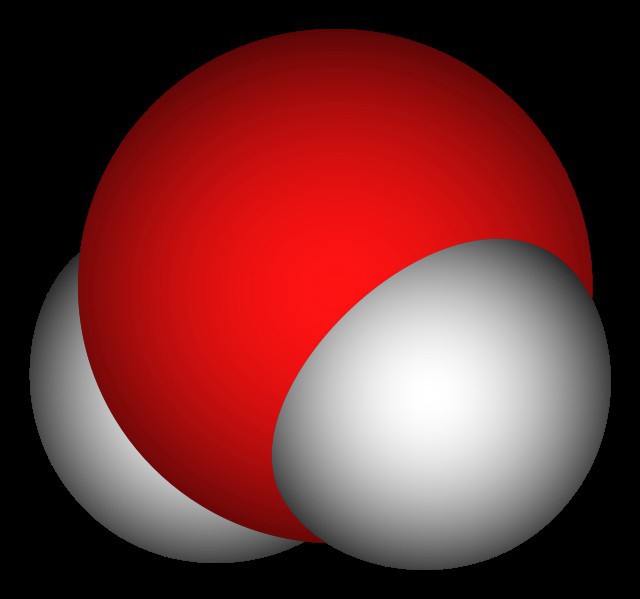
Oksijen atomunun yakınında, negatifsuçlamalar ve hidrojen atomları - pozitif. Su molekülünün hangi atomu paylaştığını bilerek, fizik onun molekülünün bir dipol olduğunu belirler. Bu tüm fiziksel özelliklerini açıklar. O, H atomlarının çekirdeği arasındaki mesafeler yaklaşık 0.1 nm'dir ve hidrojen atomları arasında - yaklaşık 0.15 nm'dir.
Aslında, su, Dünyadaki ana madde olan hidrojen oksittir. 1783'te, ünlü kimyager Lavoisier, önce su molekülünün hangi atomlara ayrıldığını gösterdiğinden, sudan hidrojen çıkardı (formül H'dir).2O). Bu nedenle molekül ağırlığı, molekülde mevcut olan oksijen ve hidrojen toplamından oluşan 18 g / mol'dür. Yapısal formül, su molekülünün hangi atomlara ayrıldığını gösterir.
Su hakkında fizik
Su, aşağıdaki özelliklere sahip, kokusu olmayan, tadı olmayan, rengi olmayan bir sıvıdır:
- su yoğunluğu - 1 g / cm3;
- donma derecesi - 0yaklaşıkC (buz);
- Kaynama derecesi - 100yaklaşıkIle (çiftleri).
Fizikteki su molekülünün hangi atomlara ayrıldığı, aşağıdaki şekle bakmak mümkündür.
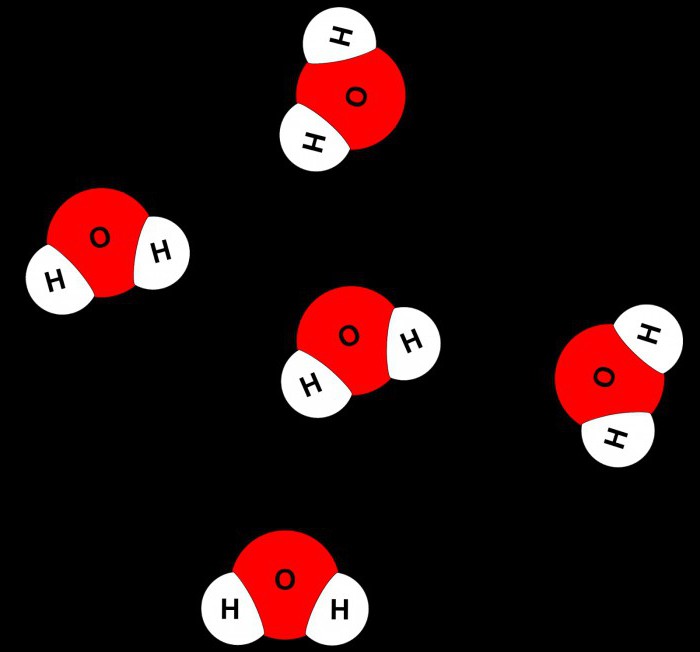
Ayrıca su en büyük yüzeye sahiptirciva hariç diğer sıvı maddelerle karşılaştırıldığında gerilim. Yüzey altında, su molekülleri kendi aralarında güçlü bir çekiciliğe sahiptir. Fakat bu moleküller üstlerindeki hava moleküllerini çekmezler, sadece birbirlerine çekilirler. Bu yüzey gerilimi, su üzerinde bir film etkisi yaratır.

Suyun kimyasal özellikleri
Su oldukça gerici bir maddedir. Onun kimyasal özellikleri su molekülünün atomlarının bölünmüş ne bağlıdır. Sıvı bir elektrik akımı etkisi altında hidrojen ve oksijen dağılır. Reaksiyon durduğu yer ve oksidan ve bir indirgeyici madde alır. Bir su molekülü çok büyük bir atom mıknatıslar gibi ve bağlanabilir neredeyse her şey ile iletişim kurabilir. tuzlarından etkisi görülmektedir altında hidroliz zayıf elektrolit elde edildi.
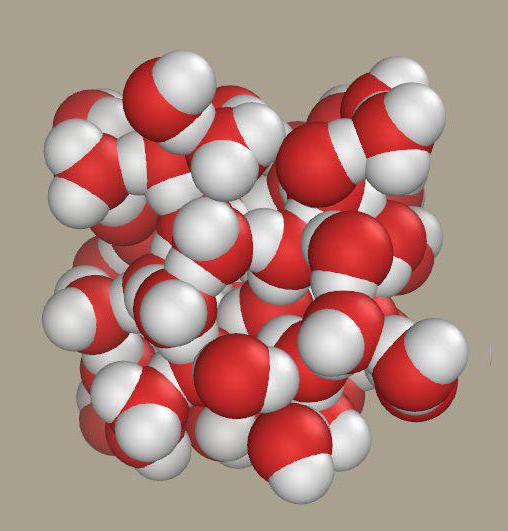
Su en bazik oksitlerle reaksiyona girer. Hidrojen salınımı olurken, örneğin sodyum, potasyum ve demir ile ısıtma gibi birçok metal ile reaksiyona girer:
2Na + 2H2O = H2 + 2NaOH;
2 K + 2H2O = H2 + 2KOH;
3Fe + 4H2O = 4H2 + Fe3Ey4.
Metal olmayanlar, metaller kadar aktif değildir, ancak güçlü ısıtma altında hala su ile etkileşirler:
C + H2O = H2 + CO;
CH4 + 2H2O = 4H2 + CO2.
Pek çok metalik olmayan oksit ile etkileşime girer. Bu durumda, bileşiğin reaksiyonları meydana gelir ve asit oluşturur.
Hidrojenin oksijen ile su buharının oluşmasıyla yanması sonucu ortaya çıkıyor:
2H2 + Hakkında2 = 2H2Oh
ve bu reaksiyon anında 700 ° C sıcaklıkta gerçekleşiryaklaşıkC.
Suda çözünme ilkesi
Sulu ortamda, toplu halde farklı birçok madde çözülebilir. Bunlar aşağıdaki türlere ayrılmıştır:
- çözünür;
- zayıf çözünür;
- neredeyse çözünmez.

Suyun işlevselliği
Gezegenimizin sakinlerinin yaşamındaki su maddesinin fonksiyonları aşırıya kaçamaz, çünkü tüm canlılar sadece onun değil, aynı zamanda bu madde sayesinde varlığını devamlı olarak sürdürürler.
- Metabolizma. Su, bir canlı organizmada meydana gelen tüm reaksiyonlar için en iyi ortam olan polar bir çözücü gibi davranır. İçinde çözünebilen maddeler hidrofilik ve çözünmez - hidrofobik olarak adlandırılır.
- Taşıma. Hücrenin iç molekülleri sürekli olarak bir hücreden diğerine geçerler. Su, herhangi bir organizmanın iç ortamındaki en önemli aktarımdır.
- Termoregülasyon. Su, ısıyı ve soğuğu eşit olarak dağıtır, vücudun içindeki sıcaklığı düzenler, örneğin hayvanlarda terlemeye neden olur, böylece vücudu soğutur.
- Suyun biyolojik değeri, vücudun birçok kimyasal reaksiyonuna katıldığı gerçeğinde yatmaktadır.
- Mekanik fonksiyon. Suyun özelliği, organ ve dokuların şeklini korumak için çok fazla küçülmez.
Olağandışı su özellikleri
Dünyada daha önemli olan hiçbir madde yoktur.tüm canlılar için, basit sudan. Değişken yoğunluk, yüksek ısı kapasitesi ve geniş yüzey gerilimi, hafıza kapasitesi su gibi bir maddenin anormal özellikleridir. Gözlemler ve deneyler, su maddesinin, içinde bir kez çözünen maddelerin özelliklerini emebilme yeteneğine sahip olduğunu ve bu malzemelerin tamamen çıkarılmasından sonra bile bu özellikleri sakladığını kanıtlamaktadır. Bu homeopatik tıbbın temel prensiplerinin temelidir. Ve bilimin bakış açısından açıklanamaz ve aynı zamanda açıklanamaz bir gerçek, muazzam enerji içeren Epiphany suyunun eşsiz iyileştirici özellikleridir. Bütün bu bulmacalar hala modern ve gelecekteki bilim adamları tarafından çözülmelidir.
</ p>



